Guida su come realizzare zucche fluorescenti e fuoco colorato
Come si realizzano le zucche fluorescenti e il fuoco del camino colorato?
Ti sei mai chiesto come mai le fiamme possano avere colori diversi, giallo, rosso, arancio, ma anche blu e verde? Com’è possibile che certi materiali restituiscano luce una volta che si fa buio con fenomeni di fosforescenza? E com’è possibile che altri materiali riflettano una luce abbagliante per fosforescenza?
Abbiamo realizzato una guida in cui coinvolgere i bimbi per divertirci con diversi materiali e tanti colori!
In merito alla fluorescenza e alla fosforescenza abbiamo già discusso nell’articolo: fluorescenza e fosforescenza: significati e differenze.
Come si realizza il fuoco colorato?
Oggi parliamo di fuoco colorato. Questo è il principio con cui si realizzano fuochi d’artificio.
Il colore della fiamma dipende dalle sostanze che impregnano il legno o il materiale che sta bruciando.
In particolare il colore dipende principalmente dai sali inorganici che impregnano il legno.
Lo ione positivo, in caso di metalli alcalini o alcalino-terrosi o alcuni metalli di transizione, in particolare, bruciando (eccitato termicamente) emette una certa lunghezza d’onda tale per cui la fiamma risulta di un determinato colore.
Come vedremo, i prodotti che si possono utilizzare per colorare il fuoco sono prodotti di uso comune reperibili nelle abitazioni o supermercati, ferramenta e negozi di giardinaggio.
In questo video abbiamo utilizzato i seguenti sali: rame solfato, rame cloruro, potassio cloruro e sodio cloruro (sale da cucina). I passaggi per la realizzazione del fuoco colorato prevedono di lavorare all’aperto, l’utilizzo di guanti, occhiali di protezione e mascherina e naturalmente la presenza di un adulto.
Materiali e metodi per fuoco colorato:
- Guanti, occhiali e mascherina;
- prodotti chimici (sale da cucina, potassio cloruro, rame cloruro e rame solfato);
- legno e carta da impregnare;
- secchi per impregnare il legno nella soluzione dei diversi sali;
- tempo di asciugatura di 2 o 3 giorni.

Per realizzare i blocchi di paraffina con i sali:
- prodotti chimici;
- guanti, occhiali e mascherina;
- occorrente per bagno maria;
- paraffina.

Sciogliere la paraffina a bagnomaria, colare la paraffina in stampi per candele contenenti i sali, se possibile mescolare con uno stuzzicadenti finchè la paraffina è bollente e liquida. Lasciar solidificare.
Passaggi per realizzare fuoco colorato:
- Abbiamo realizzato delle soluzioni con 125 g di sostanza in due lt di acqua;
- in queste quattro soluzioni abbiamo messo a bagno per circa 36 ore legno e carta;
- legno e carta sono stati lasciati asciugare in ambiente asciutto per tre giorni;
- abbiamo realizzato dei blocchi di paraffina con all’interno circa la metà in volume dei singoli sali;
- abbiamo preso un paio di legni e legnetti e carta per ciascuna soluzione e messi in un mastello;
- abbiamo dato fuoco alla carta nel mastello, alimentato il fuoco con aria in modo che anche il legno si incendiasse;
- infine abbiamo inserito la paraffina con i sali per prolungare ed intensificare la colorazione.
Significato chimico della fiamma colorata
Addentrandoci nella chimica per i più grandicelli:
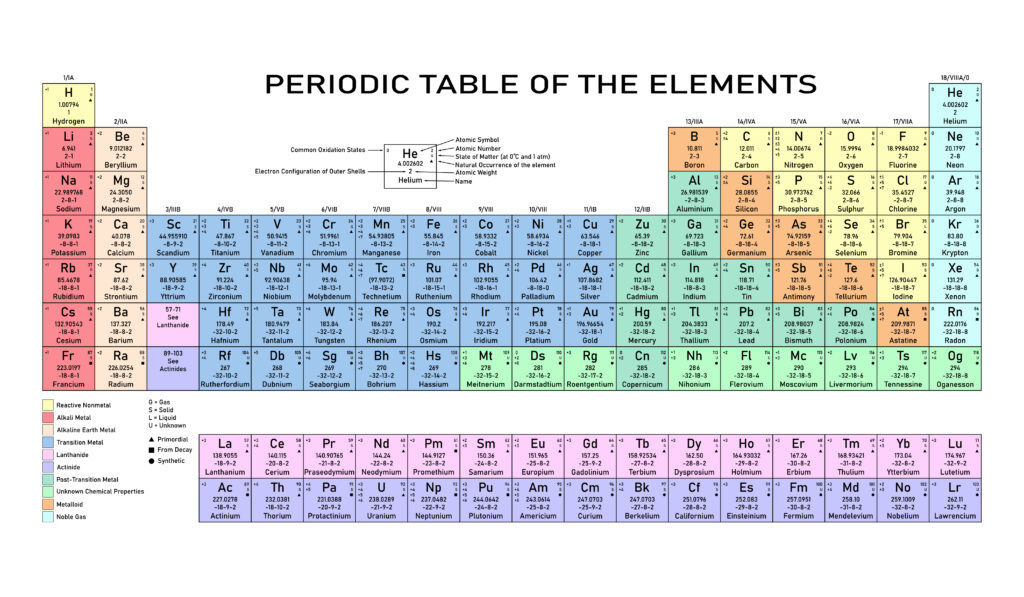
Le sostanze in grado di emettere fiamma colorata si trovano nelle prime due colonne di sinistra. Si chiamano metalli alcalini e metalli alcalino-terrosi. Anche alcuni metalli di transizione (parte centrale della tavola periodica, in blu nella tabella qui sopra) come il rame ad esempio, sono in grado di emettere fiamma colorata.
Gli atomi di questi metalli eccitati termicamente, acquisiscono energia che si traduce in un salto degli elettroni da uno stato fondamentale ad uno stato eccitato. Quando tutto torna alla normalità gli elettroni tornano allo stato fondamentale emettendo energia sotto forma di luce. Tale luce avrà una certa lunghezza d’onda caratteristica tale per cui la fiamma risulta di un determinato colore.
In chimica questo esperimento permette di dimostrare che gli elettroni possono raggiungere stati di eccitazione e tornare allo stato fondamentale. Sperimentalmente, a scuola, si riproduce questo esperimento con la tecnica del saggio alla fiamma.
I colori emessi dalle diverse sostanze
Colore – Prodotto
- Blu, Cloruro di rame (sale di rame, viene utilizzato spesso in pirotecnica per la colorazione dei fuochi, dona un colore blu/verde)
- Rosso, Cloruro di stronzio (si presenta di forma bianca ed inodore, impartisce alla fiamma un colore rosso a sprazzi)
- Giallo, cloruro di sodio (altro non è che il nostro comunissimo ed economicissimo sale da cucina)
- Viola, Cloruro di potassio (reperibile tranquillamente e senza problemi da qualunque rivenditore di prodotti chimici)
- Verde, Solfato di rame (largamente usato in agricoltura lo possiamo reperire in qualunque consorzio agricolo)
- Arancione, Cloruro di calcio (possiamo acquistarlo sotto forma di additivo alimentare con il codice europeo E509, possiamo trovarlo anche nei prodotti per assorbire umidità negli ambienti)
- Carminio, Cloruro di litio (curiosità, negli anni quaranta del secolo scorso l’industria alimentare per un breve periodo lo utilizzo al posto del cloruro di sodio o come sostituto di questo, la comparsa di sintomi di intossica mento ne fermò la commercializzazione)
Riferimenti esterni:



